研究活動
- 1.骨リモデリングの制御機構の解明
- 2.骨が産生するオステオカインの同定とその機能解析
- 3.メカニカルストレス感受・応答分子の同定と骨制御機構の解明
- 4.病態モデルを用いた治療応用の検討
骨代謝は、内分泌系だけでなく、免疫系のような他の生体制御系とも深く関連しながら制御されている。本分野では、骨構成細胞による骨リモデリング制御の解明、骨と多臓器の連環システムの解明を目指した研究を推進している。特にゲノムワイドなスクリーニング法や遺伝子改変マウスを用いた解析を展開し、分子生物学的な基礎研究から臨床応用研究まで幅広いテーマで研究を行っている。
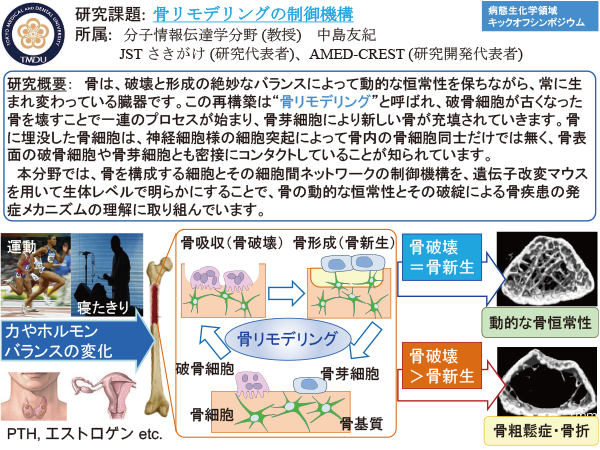
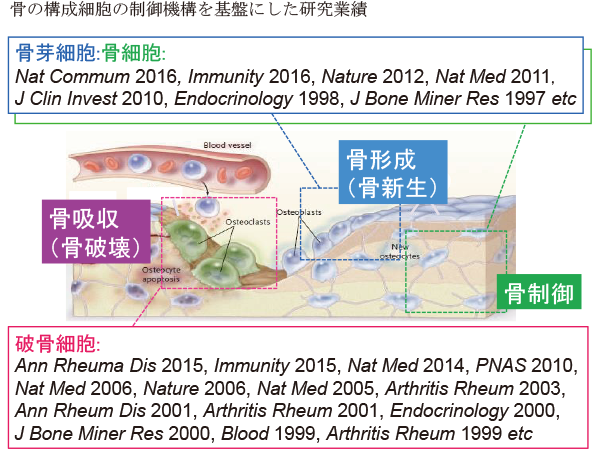
骨は、破壊と形成の動的な恒常性により、常に新しく作り替えている。この再構築は骨リモデリングと呼ばれ、強靭な骨組織の維持のみならず、生命維持に必須なミネラルの代謝器官である骨を巧妙に制御している。骨を構成する細胞、破骨細胞、骨芽細胞、骨細胞は、細胞間コミュニケーションによって骨リモデリングを制御しており、この制御機構の解明が様々な骨疾患を理解する上で重要な鍵となる。我々はトランスクリプトームやプロテオーム解析を展開し網羅的な遺伝子· タンパク発現を明らかにし、骨構成細胞の分化、機能発現の解明に取り組んでいる。
これまで、骨は、主として単純に生体を支え、運動を可能にする硬い組織という認識であった。しかし、近年の研究によって、骨は能動的に全身の機能を制御している事が示唆されるようになってきた。我々は、骨産生分子が、全身性の生体システムに連関することを実証し、責任分子(ホルモンやサイトカイン等) の同定とその機能解析を行っている。これらの解析によって、骨が多臓器を制御するネットワーク「オステオネットワーク」の全貌解明を目指している。
「骨は力学的環境に適した形状と量に調節される」(Wolff の法則)と提唱されているが、外界からのメカニカルストレスを感受し骨形態と骨量を決定する分子機構は、殆ど解明されていない。また、骨構成細胞の1つである骨細胞は、その形態学的な特徴から、骨代謝を制御する指令細胞としての可能性が示唆されているが、その機能は不明である。我々は骨細胞の機能の解明、さらに骨細胞のメカニカルストレス感受· 応答機構の解明を行っている。
細胞内シグナル伝達経路の研究の重要性は単に科学的な意義だけではない。この中から、新たな治療標的分子を見つけ、分子標的治療のモデル実験を行うことで、創薬への手がかりがつかめる。関節リウマチや骨粗鬆症のモデルマウスに対して、siRNA やウイルスベクターを用いた治療実験を行うことで、基礎研究にとどまらず臨床応用を視野にいれた研究を推進している。
教育活動
分子細胞生物学を基盤として、生体高次機能や組織形成を司る細胞内および細胞相互のシグナル伝達機構について講義する。特に、硬組織を担う骨構成細胞(破骨細胞、骨芽細胞、骨細胞)の分化機構や細胞間クロストークの制御、骨と多臓器の連環システムに焦点をあてる。また、臨床的な視点も重視し、歯周病や関節リウマチなどの炎症性骨破壊疾患や骨粗鬆症への治療応用を視野に入れたシグナル伝達についての教育を行う。